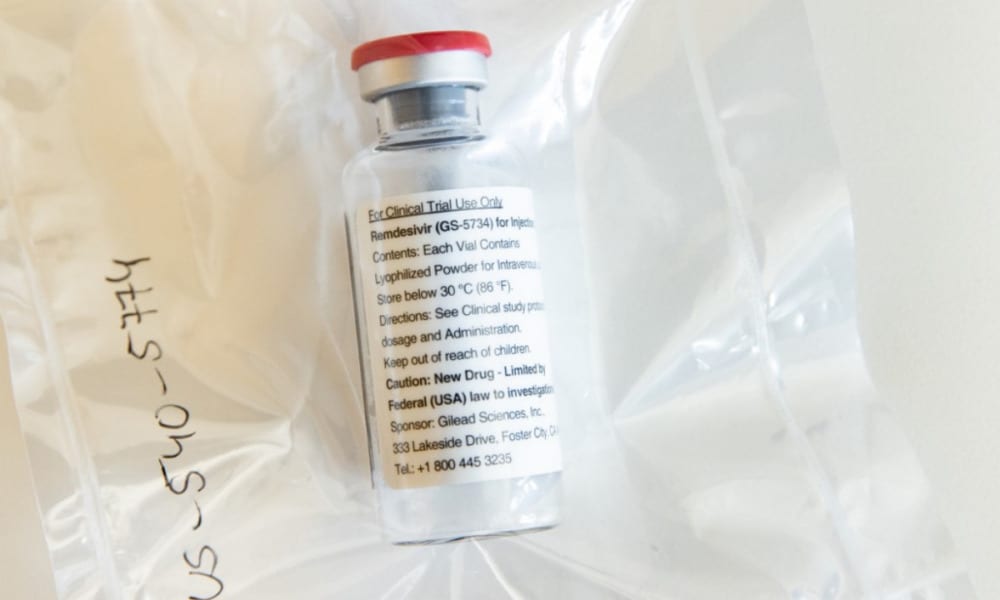
Capacidad de producción de remdesivir preocupa a la Unión Europea
La Unión Europea (UE) dijo este lunes que estudia la manera de que Gilead Sciences aumente su capacidad de producción de remdesivir, el único fármaco al que el bloque ha concedido una autorización de comercialización condicional para su uso en pacientes con COVID-19.
La comisaria europea de Salud, Stella Kyriakides, se reunió con Gilead para conversar sobre la compra del medicamento por parte de los miembros de la UE y solicitar información sobre la capacidad de producción y plazos de entrega. Las negociaciones fueron confidenciales.
Las discusiones sobre el remdesivir se producen ante un alza en las preocupaciones sobre su disponibilidad, luego que Estados Unidos informó la semana pasada que se había hecho con casi todos los suministros para los próximos tres meses.
Países como Alemania, Reino Unido y Suiza externaron que cuentan con los suministros suficientes, en medio de crecientes preocupaciones sobre el acceso a los tratamientos y vacunas para tratar la pandemia.
Gilead tiene la obligación de poner el tratamiento a disposición de los ciudadanos europeos que asumieron el riesgo de participar en ensayos humanos sin conocer los riesgos, según Andrew Hill, investigador de la Universidad de Liverpool, citado por Bloomberg.
El remdesivir logró el viernes la autorización para su uso condicional en la UE tras recibir la luz verde de la Comisión Europea.
El ministro de Salud de Alemania, Jens Sphan, señaló este lunes que el país está trabajando para asegurar que el fármaco pueda ser producido en Europa, pues aumentar la disponibilidad del fármaco no basta con adquirir dosis de la empresa, sino que se debe trasladar la producción al continente.
Spahn instó a Gilead a que garantizara suficientes suministros a Europa y dijo que había abordado el asunto con el secretario de Salud de Estados Unidos y con la empresa.
Con información de Reuters






